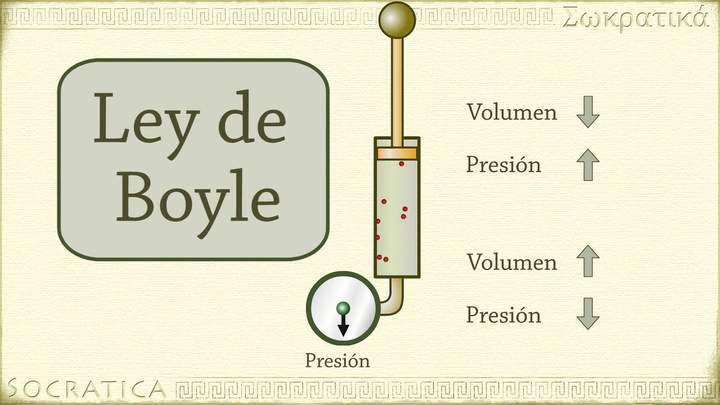
Para los gases, la presión y el volumen son inversamente proporcionales. Si mantienes todo lo demás constante y elevas la presión de un gas, su volumen disminuye. Y mientras crece el volumen que ocupa un gas, la presión se reduce.
¡No olvides suscribirte así no te pierdes la siguiente clase de química!
http://www.youtube.com/subscription_center?add_user=SocraticaEspanol
Haz click para ver más clases de química de esta lista de reproducción:
https://www.youtube.com/watch?v=qzXvNh-mwys&list=PLQlblYUWela4U_YD203iuFtLgG06td-pI
Prueba nuestra App de Tabla Periódica: la bajas GRATIS de Google Play Store:
https://play.google.com/store/apps/details?id=com.socratica.mobile.chemistry&hl=en
Presentadora: Liliana de Castro
Escrito y producido por Kimberly Hatch Harrison
¡No olvides suscribirte así no te pierdes la siguiente clase de química!
http://www.youtube.com/subscription_center?add_user=SocraticaEspanol
Haz click para ver más clases de química de esta lista de reproducción:
https://www.youtube.com/watch?v=qzXvNh-mwys&list=PLQlblYUWela4U_YD203iuFtLgG06td-pI
Prueba nuestra App de Tabla Periódica: la bajas GRATIS de Google Play Store:
https://play.google.com/store/apps/details?id=com.socratica.mobile.chemistry&hl=en
Presentadora: Liliana de Castro
Escrito y producido por Kimberly Hatch Harrison
Video
Enlace externo
Descripción
Química: Ley de Boyle (relación entre presión y volumen)
Clasificaciones
Formato
Cursos / Niveles
Asignaturas / Ámbitos
Eje
Licenciamiento
Licencia Youtube
Objetivos de aprendizaje del recurso
Objetivo de aprendizaje CN07 OA 13 CN07 OA 13
Investigar experimentalmente y explicar el comportamiento de gases ideales en situaciones cotidianas, considerando:
- Factores como presión, volumen y temperatura.
- Las leyes que los modelan.
- La teoría cinético-molecular.